Бессмертные обезьяны? Не совсем, но учёные только что обратили вспять процесс старения с помощью «супер» стволовых клеток
_____

Ключевые моменты:
- «Суперстволовые клетки» улучшили память у обезьян и обеспечили защиту от нейродегенерации. Они остановили возрастную потерю костной массы и восстановили жизнеспособность более чем половины из 61 исследованной ткани.
- Терапия также уменьшила вредное воздействие воспалений и снизила количество сенесцентных клеток — старых, не делящихся клеток, которые ускоряют старение всего организма.
- Открытие, которое может оказать существенное влияние на процесс старения, сделало учёных из Пекина на шаг ближе к тому, что раньше казалось невозможным: возвращению старым животным биологического возраста. Исследование было опубликовано в прошлом месяце в журнале Cell.
Укрепив стволовые клетки человека с помощью гена, который долгое время считался связанным с долголетием, они омолодили старых обезьян — улучшили память, защитили кости, сняли воспаление и восстановили активность десятков органов, как в молодости.
Несмотря на то, что работа проводилась на животных, она является одним из самых убедительных доказательств того, что старение у приматов может быть обратимым.
Наука, стоящая за этим прорывом
В основе исследования лежат мезенхимальные клетки-предшественники (mesenchymal progenitor cells — MPC) — тип стволовых клеток, которые содержатся в костном мозге и соединительных тканях. Эти клетки выполняют функцию поддержания организма, они способны превращаться в костные, хрящевые, жировые и мышечные клетки, а также выделять факторы, которые помогают близлежащим тканям восстанавливаться.
Но, как и все клетки, MPCs стареют вместе с нами и в конце концов подвергаются старению — состоянию перманентного выхода на пенсию. Стареющие клетки больше не делятся. Хуже того, они выделяют воспалительные молекулы, сигналы о рубцовой ткани и другие «токсичные вещества», которые ускоряют старение соседних клеток. По сути, стареющие клетки способствуют ухудшению состояния.
Но, как и все клетки, MPCs стареют вместе с нами и в конечном итоге впадают в сенесцентность — состояние перманентного «выхода на пенсию». Сенесцентные клетки больше не делятся. Что хуже, они выбрасывают воспалительные молекулы, сигналы, ведущие к образованию рубцовой ткани, и другой «токсичный шум», который ускоряет старение соседних клеток. По сути, сенесцентные клетки распространяют упадок.
Модернизация системы ремонта с помощью FoxO3
Чтобы преодолеть это истощение, исследователи обратились к белку FoxO3, известному как регулятор генов долголетия. В здоровых молодых клетках FoxO3 действует как диспетчер, включая системы ремонта ДНК, антиоксидантной защиты и программы устойчивости к стрессу. В старых клетках активность FoxO3 снижается, что делает их уязвимыми к повреждениям.
Гидра, пресноводный организм, способный к практически бесконечной регенерации, в значительной степени полагается на FoxO для поддержания активности своих стволовых клеток. У людей есть этот же белок, и генетические исследования связывают определенные варианты гена FOXO3 с исключительным долголетием.
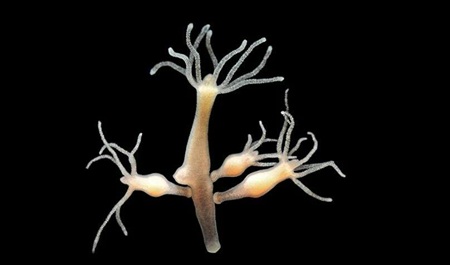
Бессмертная гидра.
Команда из Китайской академии наук генетически модифицировала MPCs таким образом, чтобы FoxO3 оставался постоянно активным внутри ядра, постоянно включая защитные гены.
Исследователи создали клетки, устойчивые к старению/сенесцентности (SRCs), изменив гены, контролирующие репарацию/восстановление ДНК, устойчивость к стрессу и функцию митохондрий. Эти усиленные клетки затем пересадили пожилым макакам, чей возраст примерно соответствовал человеческому в 60–70 лет.
Они обнаружили, что лечение с помощью SRC замедляет возрастное уменьшение объёма мозга и омолаживает множество органов и тканей.
Проще говоря: MPC обеспечивали аппаратную часть — естественную команду по восстановлению организма, — а FoxO3 представляла собой обновление программного обеспечения, которое делало их устойчивыми к старению.
Что произошло внутри обезьян
Результаты были поразительными:
Здоровье костей: Как правило, у пожилых приматов наблюдается прогрессирующая потеря костной массы, что является аналогом остеопороза у людей. У обезьян, получавших SRC, плотность костной ткани сохранилась или даже улучшилась, что позволяет предположить, что лечение обратило вспять процесс разрушения скелета.
Когнитивные способности: При выполнении заданий на память и обучение обезьяны, получавшие лечение, показали значительно лучшие результаты, они лучше запоминали предметы и эффективнее ориентировались в лабиринтах, чем их сородичи, не получавшие лечения.
Воспаление: Анализы крови выявили резкое снижение маркеров воспаления. Поскольку хроническое воспаление, которое иногда называют «инфламэйджинг» (inflammaging) или «воспалением старения», лежит в основе многих возрастных заболеваний, это открытие предполагает, что SRCs могут помочь бороться с корнем множества расстройств.
Жизнеспособность органов: Сканирование и биопсия после лечения показали омоложение мозга, костей и даже репродуктивных органов. Исследователи считают, что этот широко распространённый эффект был вызван экзосомами — крошечными везикулами, выделяемыми стволовыми клетками, которые переносят омолаживающие белки и генетический материал в другие клетки, по сути, выступая в роли посланников молодости.
Как выразился один из ведущих учёных, Си Ван: «Мы видим признаки омоложения.»
Почему это важно
Большинство испытанных до сих пор антивозрастных стратегий — от рапамицина до имитаторов голодания — работали в основном на грызунах. Перенос этих успехов на приматов с их более долгой продолжительностью жизни и сложной физиологией был труднодостижимой целью.
Это исследование иное. Продемонстрировав функциональное омоложение у макак, оно перекидывает мост между биологией мыши и человеческим потенциалом. Полученные данные свидетельствуют о том, что старение — это не просто результат пассивного износа, а, по крайней мере, частично, программируемый и обратимый процесс.
Если аналогичные методы сработают на людях, то в будущем с помощью SRC можно будет лечить не только остеопороз или ухудшение памяти, но и сам синдром старения в целом.
Но остаётся множество вопросов
Эксперты подчеркивают, что, несмотря на многообещающие результаты, их применение в лечении людей далеко не гарантировано. Возникают вопросы:
Безопасность: Будут ли клетки, устойчивые к старению, вести себя предсказуемо или они могут существовать слишком долго, повышая риск развития рака?
Срок действия: Как долго сохраняются преимущества? Месяцы? Годы? На всю жизнь?
Доставка: Можно ли производить такие клетки в больших количествах и примет ли их организм без иммунного отторжения?
Этика: Как следует тестировать такие методы лечения на людях и у кого должен быть доступ к ним, если они работают?
«Это важный этап, но мы не должны торопиться с заголовками о бессмертии человека», — сказал независимый эксперт в области геронтологии. «Это показывает, что системное старение у приматов можно замедлить — и это уже немало».
Взгляд в будущее
На данный момент макаки продолжают находиться под наблюдением, а их тела посылают сигналы молодости благодаря пересаженным клеткам. Но последствия могут быть значительными: если учёные смогут пополнить механизм восстановления организма клетками, способными противостоять старению, медицина может перейти от лечения болезней по отдельности к устранению их общей причины.
Эта идея, которую когда-то считали научной фантастикой, теперь всё больше приближается к научной реальности.
- 717 просмотров
